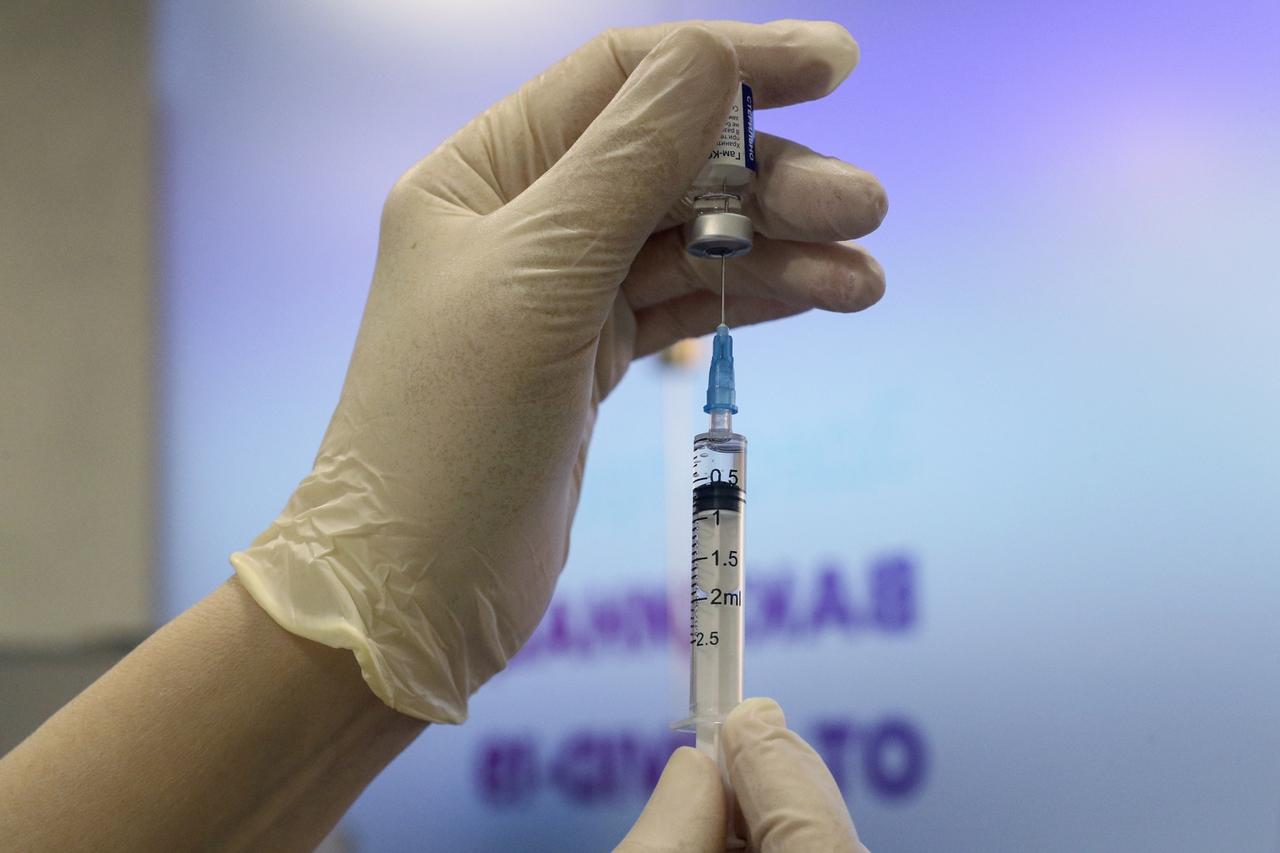
Europska agencija za lijekove počela je s postupnom ocjene Sputnjika V, ruskog cjepiva protiv COVID-19. Podnositelj je zahtjeva njemačka tvrtka R-Pharm Germany Gmbh.
Kako se navodi u priopćenju, EMA će ocijeniti sve podatke o ovom cjepivu čim postanu dostupni kako bi utvrdila jesu li koristi primjene ovog cjepiva veće od eventualnih rizika. Postupna ocjena dokumentacije o cjepivu nastavit će se dok ne bude dostupno dovoljno dokaza koji podržavaju podnošenje službenog zahtjeva za davanje odobrenja za stavljanje cjepiva u promet. Premijer Andrej Plenković rekao je jučer da je Vlada više nego pripravna nabaviti rusko cjepivo Sputnjik V kada ga Europska agencija za lijekove odobri. Plenković je na sjednici Vlade rekao da je Vlada od ruske strane zatražila dodatnu dokumentaciju o cjepivu Sputnjik V te istaknuo da je očito započeta formalna procedura da ga EMA odobri.
Sve ovisi o dokumentaciji
– Kada Agencija odobri cjepivo, mi smo više nego pripravni da ga nabavimo i dodatno stavimo u funkciju zaštite građana od pandemije – poručio je premijer. Tijekom ožujka očekuje se odobrenje EMA-e za cjepivo Johnson&Johnson, što je, rekao je, novih 900.000 doza u dolasku, u određenoj u dinamici distribucije. Objašnjeno nam je kako proizvođač lijeka mora imati nositelja odobrenja za stavljanje lijeka u promet (pojednostavljeno: zastupnika) sa sjedištem u Europskoj uniji.
– Nema još nikakvih procjena o vremenu koliko će ovaj postupak trajati do registracije, sve će ovisiti o dokumentaciji i podacima koje EMA zaprimi od podnositelja zahtjeva, odnosno o dinamici kojom će dostavljati podatke potrebne za ocjenu, te uzimajući u obzir da se proizvodnja cjepiva odvija izvan EU, zbog čega je u postupku davanja odobrenja potrebno provesti i inspekciju proizvodnih pogona kako bi se potvrdilo da udovoljavaju zahtjevima dobre proizvođačke prakse, odnosno da je u njima moguće provesti serije cjepiva koje udovoljavaju postavljenim specifikacijama i kriterijima kakvoće – rekla je Ivana Šipić Gavrilović iz HALMED-a, naše regulatorne agencije za lijekove. Ona navodi da su u EMA-i, kako bi postupak trajao što kraće, a uz zadovoljavanje svih visokih kriterija, prethodno imenovani vodeći ocjenitelji za svaki od aspekta koji se ocjenjuje (kakvoća, klinički, neklinički podaci i dr.) te su formirani multinacionalni timovi regulatornih tijela država članica koji će provoditi inspekciju dobre proizvođačke i dobre farmakovigilancijske prakse.
Što znači postupna ocjena
Kako stoji na stranicama HALMED-a, postupna ocjena dokumentacije o lijeku (engl. rolling review) jedan je od regulatornih mehanizama koji se primjenjuju u kontekstu izvanredne javnozdravstvene situacije, kao što je trenutačna pandemija bolesti COVID-19. Cilj ovog postupka jest ubrzati postupak davanja odobrenja za stavljanje u promet lijeka koji je trenutačno u istraživanju, a pokazuje potencijalnu djelotvornost. U slučaju postupne ocjene dokumentacije o lijeku, ocjenitelji CHMP-a ocjenjuju podatke iz ispitivanja koja se trenutačno provode čim oni postanu dostupni, prije nego što je podnesen zahtjev za davanje odobrenja.



























"Ivana Šipić Gavrilović iz HALMED–a: Treba provesti i inspekciju pogona u kojima se proizvodi cjepivo " a u astrazenecu i pfizeru ste bili i pokazali su vam dokumentaciju kako ga proizvode?