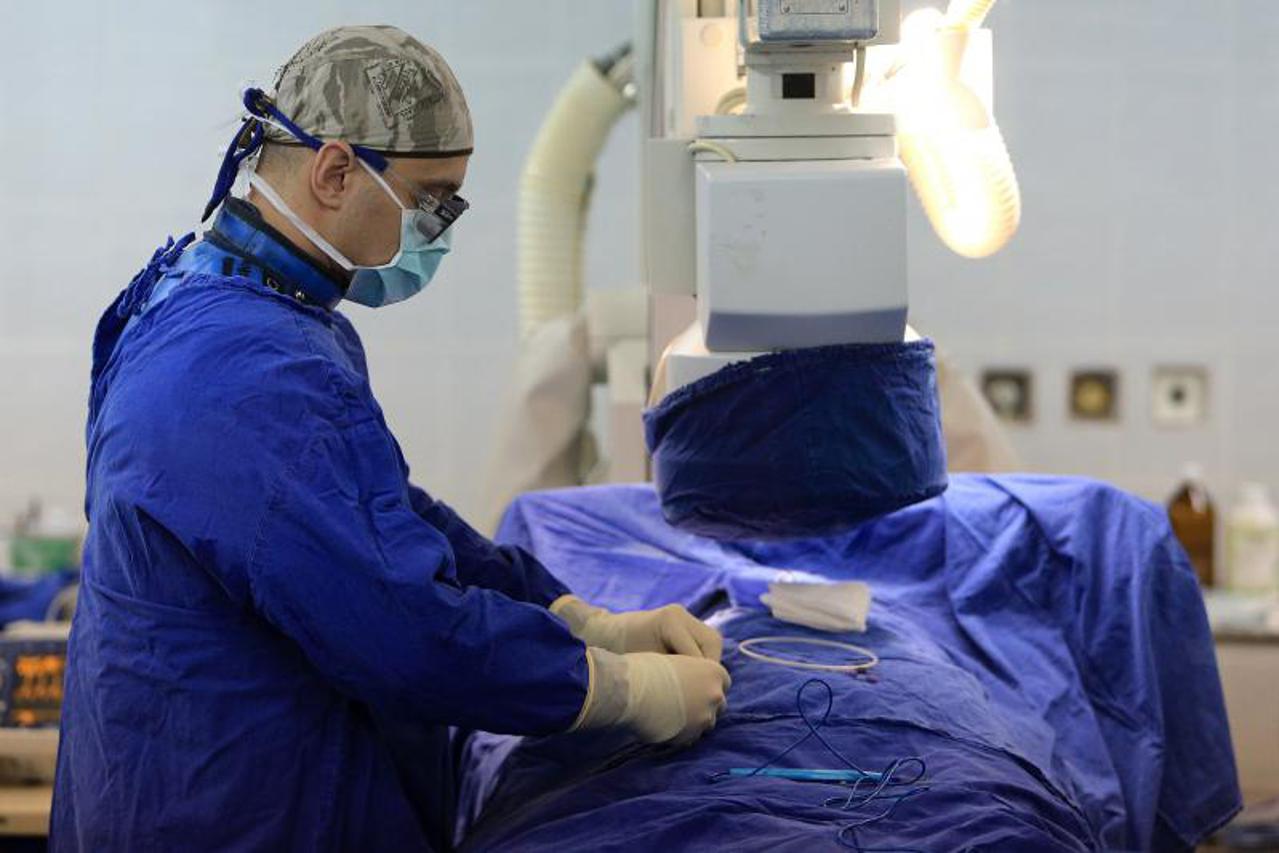
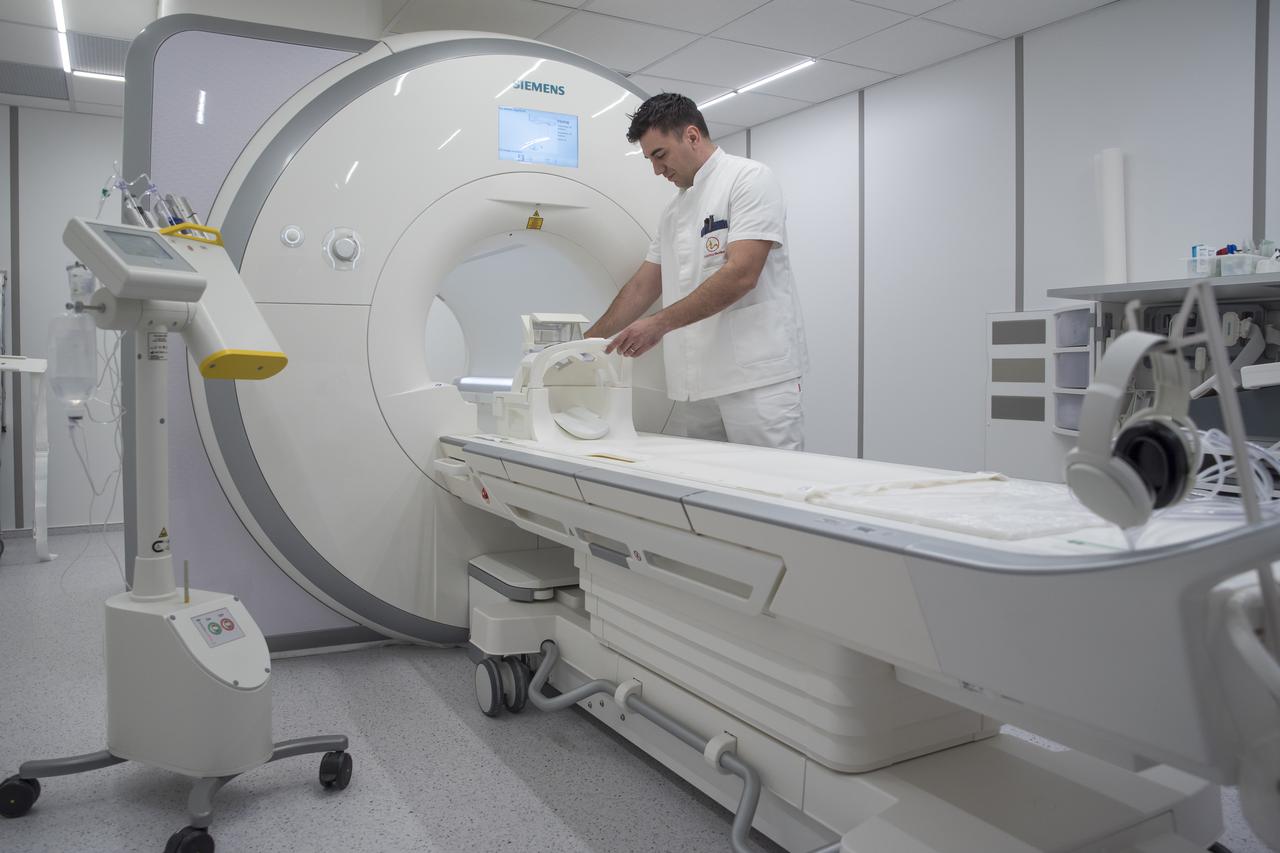
P: Bio sam na operaciji kuka koja baš i nije uspjela. Što učiniti? Tvrtko, Split
O: U tijeku je postupak donošenja rezolucije o prijedlogu uredbe Europskog parlamenta i Vijeća o medicinskim proizvodima kojim se poboljšavaju dosadašnje direktive na tržištu o medicinskim proizvodima. Nama je to prilika da se i područja koja dosad u našem zakonodavstvu nisu bila uređena konačno urede. Novi medicinski proizvodi pojavljuju se gotovo svakodnevno na tržištu, no istodobno nisu usklađena pravila za njihovo stavljanje na tržište, a često se koristi i proizvod koji nije dovoljno ispitan ili čije se manjkavosti primijete tek kasnije. Tako sigurnost pacijenata često ustupa mjesto želji da se ugradi novi proizvod, višeg standarda, ali kratkog klinički ispitanog učinka. U svakom slučaju klinika gdje ste operirani u obvezi vam je uručiti popratnu dokumentaciju iz koje ćete biti upoznati s proizvodom koji je ugrađen u vaš organizam.
Usporedno se će se pratiti sva događanja na vašim redovitim pregledima, što će biti upisano u vašem otpusnom pismu ili drugom dokumentu koji ćete primiti na liječničkom pregledu ili u slučaju da bude potrebno obaviti reoperaciju. Tada je klinika obvezna izvijestiti vas o svim činjenicama koje su joj prethodile. Tijek vašeg liječenja nakon ugradnje implantanta mora biti kontinuirano praćen, sukladno zakonskim obvezama proizvođača proizvoda i klinike koja taj proizvod ugrađuje, da bi se u slučaju komplikacija moglo dijagnosticirati uzrok komplikacije te uzročno-posljedičnu vezu s ugrađenim kukom, odnosno proizvodom. U slučaju pozitivnog nalaza i utvrđivanja postojanje uzročno-posljedične veze potrebno je obaviti dodatne dijagnostičke pretrage kako bi se utvrdile trajne posljedice te s te osnove možete pokrenuti postupak naknade štete.